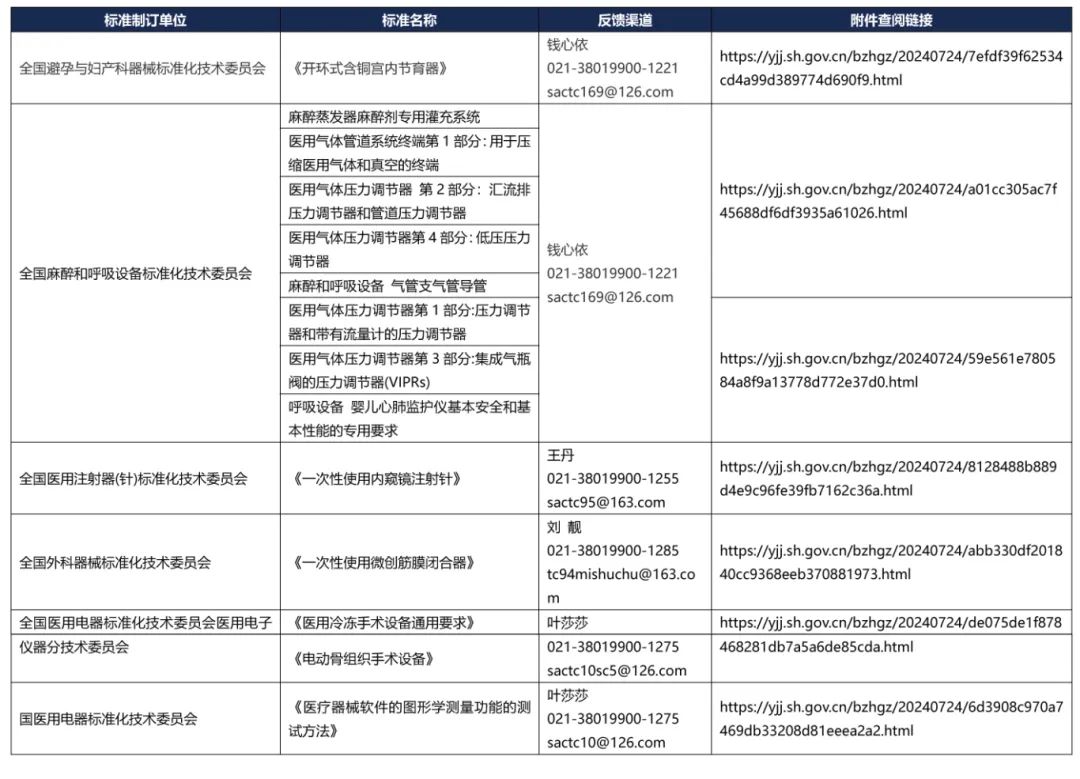
1、 近期标准征求意见的通知
2、当导管三尖瓣置换器械尺寸较大无法进行原位植入动物试验时,如何选择试验样品
由于实验用动物的解剖结构限制,导管三尖瓣置换器械成品可能无法进行原位植入的动物试验,可以选择相同生产工艺生产的等比例缩小的试样或选择合适的动物模型进行动物试验。如使用等比例缩小的试样,需提供试样合理性分析,分析尺寸差异对试验结果的影响。
3、仅有一个适用样本类型的体外诊断试剂,是否需要在申报资料CH3.5.2适用样本类型研究项下提交研究资料
如申报体外诊断试剂仅有一个适用样本类型(含抗凝剂),如EDTA-K2抗凝血浆,且所有性能研究资料均采用该样本类型,则可在CH3.5.2项下提交解释说明,无需再单独提交研究资料。如申报体外诊断试剂适用含多种抗凝剂的样本类型,如EDTA-K2抗凝血浆、肝素锂抗凝血浆,则需在CH3.5.2项下提交适用样本类型研究资料。
4、FDA发布《无菌类器械 (510(k))申报资料中无菌证明资料递交及审查》指南——器审中心官方解读
2024年1月8日,美国FDA发布《无菌类器械上市前通知(510(k))申报资料中关于无菌证明资料的递交及审查》指南文件。该指南文件阐明在无菌类器械510(k) 申报资料中应包括的灭菌过程、热原信息。器审中心于2024年7月26日对其内容发布简述,以供参考。详细内容请见原文。









































 粤公网安备 44030602000441号
粤公网安备 44030602000441号