医械资讯周刊,新鲜事简单报,安全用械,共享健康!CTI华测检测医械资讯周刊2024年6月第一期,本期要闻:关于公开征求《医疗器械分类目录》部分内容调整意见的通知、国家药监局关于注销脑动脉瘤夹等4个医疗器械注册证书的公告(2024年第69号)、2024年5月进口第一类医疗器械产品备案信息...
1、关于公开征求《医疗器械分类目录》部分内容调整意见的通知
根据《医疗器械分类目录动态调整工作程序》及相关要求,国家药品监督管理局医疗器械标准管理中心针对医疗器械分类标准22临床检验器械-15样本处理系统-05样本处理系统类设备的产品描述,预期用途和品名举例进行部分调整。
针对调整内容有建议反馈的于2024年7月1日前将《征求意见反馈表》(附件2)通过电子邮件反馈至flmsc nifdc.org.cn,邮件标题请注明反馈单位或个人名称。
2、国家药监局关于注销脑动脉瘤夹等4个医疗器械注册证书的公告(2024年第69号)
按照《医疗器械监督管理条例》规定,根据企业申请,国家药品监督管理局现注销以下3家企业共4个产品的医疗器械注册证:
一、沧州康华医疗器械有限公司的2个产品:脑动脉瘤夹,注册证编号:国械注准20163131005;颅骨修补钛网板螺钉系统,注册证编号:国械注准20173130706。
二、德国杜塞拉姆医学陶瓷有限公司的1个产品:全瓷义齿用氧化锆瓷块,注册证编号:国械注进20222170163。
三、斯派恩华医疗器械有限公司的1个产品:脊柱固定系统,注册证编号:国械注进20153132575。
3、2024年5月进口第一类医疗器械产品备案信息
国家药品监督管理局发布2024年5月进口第一类医疗器械的产品备案信息,总计包含156项医疗器械备案证的有效,变更以及无效,主要包括体外诊断(IVD)类产品,手术器械和部分患者承载器械附件等。
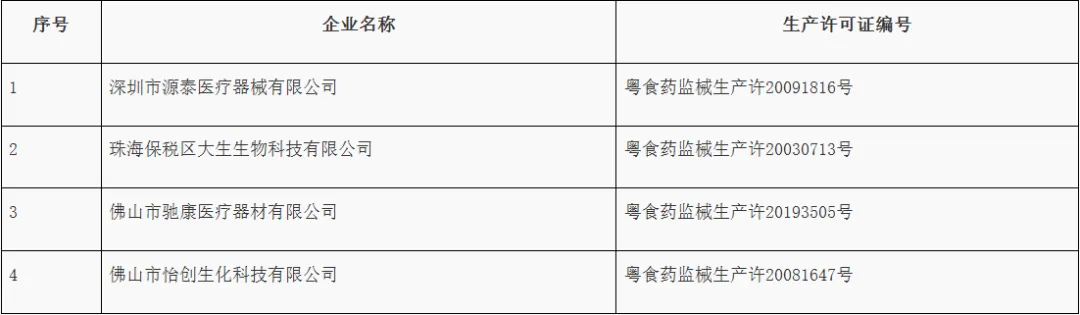
4、广东省药品监督管理局关于4家医疗器械生产企业恢复生产的通告
经广东省药品监督管理局组织复查,以下4家医疗器械生产企业已完成缺陷项目整改,符合《医疗器械生产质量管理规范》相关规定恢复生产。
5、佛山市南海凤华医疗器械有限公司对一次性无菌鼻塞吸氧管主动召回
佛山市南海凤华医疗器械有限公司生产的一次性无菌鼻塞吸氧管(粤械注准20182080995),生产批号为230417、230418,经抽检发现产品不符合技术要求,佛山市南海凤华医疗器械有限公司决定发起主动召回,召回级别为二级召回。详细信息见《医疗器械召回事件报告表》。
6、关于征集参与《二氧化碳激光治疗设备注册审查指导原则》编制工作的相关企业及单位信息的通知
医疗器械技术审评中心现已启动《二氧化碳激光治疗设备注册审查指导原则》的编制工作。目前在征集编制工作参与单位,邀请具有相关工作经验的境内外生产企业、科研机构、临床机构等积极参与。
请有意向参与编制工作的单位填写参与单位信息征集表(附件),于2024年6月30日前以电子版形式报送我中心。邮件主题请以“XX指导原则+单位名称”的格式命名。
联系人:金若男;
联系电话:010-86452643;
电子邮箱:jinrn cmde.org.cn









































 粤公网安备 44030602000441号
粤公网安备 44030602000441号