医械资讯周刊,新鲜事简单报,安全用械,共享健康!CTI华测检测医械资讯周刊2024年4月第一期,本期要闻:2024年3月进口第一类医疗器械产品备案信息...
1、2024年3月进口第一类医疗器械产品备案信息
国家药品监督管理局发布2024年三月进口第一类医疗器械产品备案信息,共涉及195种进口医疗器械备案的有效、变更以及备案失效。
2、医疗器械优先审批申请审核结果公示(2024年第5号)
依据原国家食品药品监督管理总局《医疗器械优先审批程序》(总局公告2016年168号),我中心对申请优先审批的医疗器械注册申请进行了审核。下述项目符合优先审批情形,拟定予以优先审批,现予以公示。
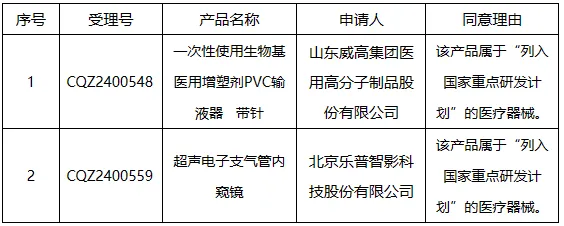
公示期内,任何单位和个人有异议的,可以填写医疗器械优先审批项目异议表,书面提交至器审中心中心综合业务部。
3、国家药监局关于进一步加强医疗器械注册人委托生产监督管理的公告(2024年第38号)
为贯彻实施《医疗器械监督管理条例》,国家药品监督管理局发布《进一步加强医疗器械注册人委托生产监督管理的公告》,公告主要包括三部分:严格落实医疗器械注册人主体责任;切实强化医疗器械委托生产注册管理;持续加强委托生产监督管理。旨在全面落实医疗器械注册人(以下简称注册人)质量安全主体责任,进一步加强注册人委托生产监督管理,有效防控医疗器械质量安全风险。
4、关于公开征集医疗器械临床评价行业标准制订项目参与单位的通知
为进一步提升标准制修订工作相关方参与程度,提高标准制修订工作质量与水平,全国医疗器械临床评价标准化技术归口单位现就2024年度拟开展的《医疗器械真实世界数据术语和定义》等2项行业标准制订项目征集参与单位,相关事宜如下:
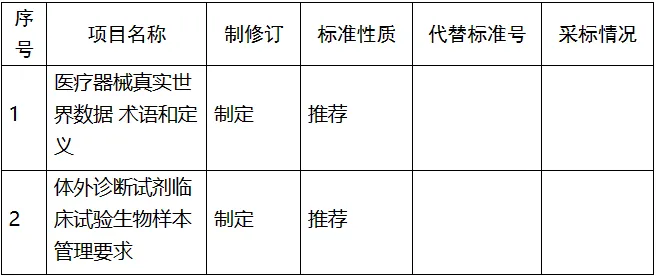
一、2024年度拟开展行业标准制修订项目
二、要求申请参与标准制定的单位:具备独立法人资格;具有与制修订标准项目相关的研究、生产、管理等工作背景和技术能力;熟悉国家医疗器械有关政策、法规、标准,熟悉医疗器械标准制修订工作流程;能充分参与标准制修订工作并完成分担的工作任务。
三、其他说明
为保质保量完成标准制修订工作,每个单位申请参与的制修订项目原则上不超过两项;本次征集工作不与标准起草单位、起草人冠名挂钩;标准编制的相关费用由参与单位自行承担。
四、申报材料
请有意报名单位填写《2024年医疗器械临床评价行业标准参与单位报名表》,并于2024年4月17日之前将报名表电子版(word版+PDF盖章扫描版)报送秘书处。









































 粤公网安备 44030602000441号
粤公网安备 44030602000441号